La Ley 14/1986, de 25 de abril, General de Sanidad, declara tener por objeto la regulación general de todas las acciones que permitan hacer efectivo el derecho de protección de la salud reconocido en el artículo 43 y concordantes de la Constitución. A su vez, en su artículo 18, entre las actuaciones concretas del sistema sanitario, se señalan los programas de atención a grupos de población de mayor riesgo, los programas de orientación en el campo de la planificación familiar y el control sanitario de los productos farmacéuticos, así como de otros productos y elementos de utilización terapéutica, diagnóstica y auxiliar, atribuyendo expresamente, en su artículo 40, a la Administración del Estado, entre otras actuaciones, las relativas a la reglamentación, autorización y registro u homologación, según proceda, de aquellos artículos que, al afectar al ser humano, puedan suponer un riesgo para la salud de las personas.
Por su parte, la Ley 25/1990, de 20 de diciembre, del Medicamento, regula los principios, normas, criterios y exigencias básicas sobre la eficacia, seguridad y calidad de los productos sanitarios, facultando al Gobierno, en su disposición adicional tercera 2, para determinar entre otros, aquellos productos sanitarios que hayan de ser autorizados por el Estado, en razón a su especial riesgo o trascendencia para la salud.
El Real Decreto 3033/1978, de 15 de diciembre, por el que se desarrolla la Ley 45/1978, de 7 de octubre, por la que se modifican los artículos 416 y 343 bis del Código Penal, clasifica los distintos anticonceptivos, diferenciando los anticonceptivos hormonales y los espermicidas de los dispositivos intrauterinos y de los medios mecánicos anticonceptivos a los que sólo regula con carácter muy general en lo relativo a su expendición, venta y publicidad.
Entre los distintos tipos de medios anticonceptivos mecánicos se encuentran los condones o preservativos de caucho, los cuales han demostrado su eficacia como tal método siempre que reúnan determinadas especificaciones de calidad y se utilicen correctamente.
La Norma UNE 53-625-89, elaborada por el Organismo de Normalización y Certificación AENOR, establece las características y métodos de ensayo de los preservativos de caucho. Se trata de una Norma en el sentido de la definición establecida en el Real Decreto 1614/1985, de 1 de agosto, por el que se ordenan las actividades de normalización y certificación, y cuya observancia no es obligatoria. Mediante el presente Real Decreto se ha estimado conveniente hacer obligatorio el cumplimiento de la citada Norma UNE para la comercialización en España de los preservativos de caucho, posibilitando a la vez su adaptación a las modificaciones o sustituciones de que aquélla pueda ser objeto.
Los condones además resultan útiles como medio de prevención de enfermedades de transmisión sexual, fines con los que han sido tradicionalmente prescritos y utilizados.
En los últimos años la aparición y propagación del SIDA se ha convertido en un gran problema de salud pública. La inexistencia de medidas de protección de aplicación general y el lento avance de los medios terapéuticos hacen que los programas de las autoridades sanitarias se orienten hacia actividades de prevención, fundamentalmente de educación sanitaria, que tengan como objetivo reducir el riesgo de infección por VIH. Entre estas actividades se encuentra la recomendación del uso del preservativo.
Todo ello justifica sobradamente la consideración del preservativo como producto sanitario y conduce a la regulación de sus condiciones de comercialización y a la definición de los requisitos que deben satisfacer para su homologación sanitaria con objeto de asegurar una adecuada fiabilidad en su utilización.
El presente Real Decreto se dicta al amparo de lo dispuesto en el artículo 149.1.16.a de la Constitución española y en virtud de los artículos 40.5 y 95, en relación con el artículo 2.º, 1, de la Ley 14/1986, de 25 de abril, General de Sanidad.
En su virtud, a propuesta del Ministro de Sanidad y Consumo, oídos los sectores afectados, previo informe favorable del Consejo Interterritorial del Sistema Nacional de Salud, de acuerdo con el Consejo de Estado y previa deliberación del Consejo de Ministros, en su reunión del día 22 de noviembre de 1991,
DISPONGO:
TÍTULO PRIMERO
Objeto y ámbito de aplicación
1. El presente Real Decreto establece las condiciones técnico-sanitarias que deben reunir los preservativos de caucho (condones), para su comercialización en España, contengan o no espermicidas u otras sustancias.
2. Los mencionados condones tendrán la consideración de productos sanitarios, a los efectos previstos en la Ley 25/1990, de 20 de diciembre, del Medicamento.
1. Los preservativos de caucho cumplirán las especificaciones técnicas que figuran en el anexo I al presente Real Decreto, y que corresponden a las contenidas en la Norma UNE 53-625-89. «Elastómeros. Preservativos de caucho (condones). Características y métodos de ensayo».
2. Las mencionadas especificaciones técnicas se adaptarán a las contenidas en las normas que, en su caso, modifiquen o sustituyan a la mencionada UNE 53-625-89.
3. Las sustancias activas añadidas al condón deben haber demostrado su actividad para la indicación y propiedades que persigue su incorporación al mismo.
4. La fabricación, almacenamiento y control de los condones se realizará en instalaciones que posean los medios necesarios para garantizar la calidad del producto terminado.
1. Para proceder a la comercialización de los preservativos, éstos deberán estar previamente homologados por la Dirección General de Farmacia y Productos Sanitarios de acuerdo con los criterios establecidos en este Real Decreto.
2. La Dirección General de Farmacia y Productos Sanitarios asignará un número de homologación a cada producto y extenderá el documento acreditativo pertinente cuando se verifique que aquél cumple todas las condiciones contempladas en la presente disposición. Esta verificación podrá requerir la inspección de las instalaciones del fabricante o del importador o del acondicionador, en su caso.
3. La Dirección General de Farmacia y Productos Sanitarios podrá proceder a la homologación de los condones procedentes de otros Estados miembros de la Comunidad Europea sobre la base de la documentación que presente el solicitante y que certifique que los productos cumplen la reglamentación en vigor en el país de origen y que han sido fabricados conforme a normas técnicas que permitan asegurar un nivel de seguridad y fiabilidad equivalente al que permiten alcanzar las normas españolas.
4. La concesión de la homologación sanitaria se entenderá otorgada transcurrido el plazo de tres meses a contar desde la fecha de presentación de la solicitud, siempre que los interesados presenten sus peticiones debidamente documentadas y los productos se ajusten a lo dispuesto en los títulos II, III y IV del presente Real Decreto.
El requerimiento de cualquier documentación adicional, aclaración o precisión por parte de la Dirección General de Farmacia y Productos Sanitarios paralizará el transcurso de dicho plazo hasta la recepción de lo solicitado.
5. La homologación será temporal y agotada su vigencia deberá revalidarse.
6. Las homologaciones y sus suspensiones, revocaciones y cancelaciones, cuando sean firmes, serán publicadas en el «Boletín Oficial del Estado», mediante referencia a su objeto, fecha, titularidad y período de validez.
1. Con antelación a la puesta en el mercado de sus artículos las Empresas deberán comunicar a la Dirección General de Farmacia y Productos Sanitarios, cualquier modificación producida en la composición, características o presentación de los mismos, o en sus procedimientos de fabricación y control. Igualmente comunicarán los posibles cambios de fabricante o acondicionador de sus productos.
2. Cuando las modificaciones introducidas puedan afectar al cumplimiento de las condiciones técnicas o sanitarias se requerirá su previa verificación y aprobación.
3. La retirada o caducidad de las marcas de conformidad o certificados señalados en el artículo 5.º, 1.4, deberán ser puestas en conocimiento de la Dirección General de Farmacia y Productos Sanitarios por la Empresa titular de la homologación.
1. Para proceder a la homologación, el fabricante y/o importador formulará la correspondiente solicitud, ante la Dirección General de Farmacia y Productos Sanitarios, presentando los siguientes documentos:
1. Escrito de solicitud según modelo establecido al efecto en el anexo II al presente Real Decreto. Una misma solicitud sólo podrá amparar artículos que posean las mismas características de diseño de las señaladas en el apartado 4.2 del anexo I y la misma composición en las sustancias añadidas al preservativo y que estén fabricados por la misma Entidad.
2. Memoria técnica en la que figurarán los siguientes datos:
a) Descripción detallada del artículo: Diseño, tipo, color, dimensiones y características físicas.
b) Descripción del proceso de fabricación, indicando, si procediera, composición y finalidad de las sustancias añadidas al preservativo. En el caso de que alguna de las fases de fabricación, incluido envasado y etiquetado, no se realizará en las mismas instalaciones deberán indicar las condiciones en que se efectúa el transporte de los artículos.
c) Controles de calidad en materias primas y material de envasado, en proceso de fabricación y en producto terminado. Periodicidad de los mismos.
d) Fecha de caducidad prevista para el artículo basada en los resultados obtenidos en el ensayo de estabilidad durante el almacenamiento referenciado en el anexo I.
e) Significado de la clave de identificación del lote de fabricación que podrá a su vez identificar al fabricante.
f) Clave de identificación del fabricante en caso de no estar implícita en la del lote de fabricación.
g) Si el condón contiene sustancias activas deberán aportar además documentación que avale las propiedades de estas sustancias y su adecuación par ser utilizadas con el preservativo.
3. Etiquetas o cartonajes de cada una de las marcas comerciales de los artículos a homologar que deberán ajustarse a lo establecido en el artículo 8.º
4. Documento acreditativo del cumplimiento de las especificaciones reseñadas en el artículo 2.º, 1 y 2. A tal efecto se aceptará cualquiera de los documentos siguientes:
a) Fotocopia autenticada del certificado extendido por la Asociación Española de Normalización y Certificación (AENOR), de la concesión de la marca AENOR para el producto del que se solicita la homologación.
b) Certificado de conformidad a las especificaciones técnicas que figuran en el anexo I, emitido por un Laboratorio acreditado a tales efectos por el Ministerio de Sanidad y Consumo.
2. Los preservativos que hayan obtenido la correspondiente marca de conformidad concedida por AENOR podrán ser objeto de comunicación directa por parte de esta Entidad a la Dirección General de Farmacia y Productos Sanitarios a los efectos previstos en el artículo 3.º del presente Real Decreto, acompañando el documento a que se refiere el apartado anterior en su número 4, a), y la documentación técnica que soporte la concesión de dicha marca, quedando eximidos del procedimiento descrito en el citado apartado.
La Dirección General de Farmacia y Productos Sanitarios asignará, en su caso, un número de homologación a dichos productos y extenderá el documento acreditativo pertinente a favor del interesado, remitiendo copia del mismo a AENOR.
3. Cuando se trate de artículos importados de países no miembros de la Comunidad Europea se incluirá, además:
a) Certificado de representación del fabricante extranjero a favor del importador en España.
b) Certificado de libre venta o certificación emitida por las autoridades sanitarias que acredite que el artículo cumple la legislación sanitaria vigente en el país de origen.
4. Cuando un mismo expediente de homologación ampare a productos fabricados en instalaciones diferentes de la misma Entidad fabricante, los documentos citados harán referencia a cada una de las plantas de fabricación.
La Dirección General de Farmacia y Productos Sanitarios podrá denegar o revocar la homologación cuando resulte:
a) Que exista incumplimiento de las especificaciones técnicas y las condiciones sanitarias.
b) Que las condiciones de fabricación o los métodos de control de calidad aplicados por el fabricante no garanticen el mantenimiento homogéneo de las características técnicas y sanitarias.
c) Que el envasado y acondicionamiento no garanticen el mantenimiento de las características técnicas y sanitarias hasta el momento de utilización o que el etiquetado no sea suficiente para asegurar su correcta utilización.
d) Que existan indicios racionales de que la utilización del producto pueda ir en perjuicio de la salud del usuario o la salud pública.
e) Que sean retiradas las certificaciones mencionadas en el artículo 5.º, 1.4.
f) Que hayan variado las condiciones en que fue emitida la homologación sin la oportuna comunicación o aprobación.
1. Cada preservativo deberá disponerse en un envase individual. Uno o más envases individuales deberán disponerse en un envase comercial.
2. Los envases de los preservativos deberán reunir las condiciones especificadas en el apartado 8.2 del anexo I, correspondiente a embalaje.
3. Cuando los envases comerciales no sean preparados por el propio fabricante de los condones el responsable del empaquetado y embalaje conservará los datos necesarios para identificar el fabricante y el lote del artículo.
1. En los envases de los condones deberán figurar, con caracteres fácilmente legibles e indelebles, al menos en la Lengua Española Oficial del Estado, como mínimo, los siguientes datos:
a) En el envase individual:
Los señalados en el apartado 8.3.1 del anexo I y además:
– Fecha de caducidad, expresada en mes y año.
b) En el envase comercial:
Los señalados en el apartado 8.3.2 del anexo I con excepción del previsto en la letra h) y además:
– Dirección del fabricante y/o importador o acondicionador, según proceda.
– En caso de condones que contengan sustancias activas, la leyenda: «Contiene espermicida», «Contiene retardante...», o similar.
– La leyenda «Homologado en la DGFPS número ... CC».
– Indicaciones para su desecho, que figurarán en el propio envase o en hoja aparte incluida en el mismo.
2. Las alusiones relativas a la prevención de enfermedades de transmisión sexual deberán proporcionar una información real sobre las expectativas que el preservativo ofrece.
Por los Servicios de Inspección y Control de las Administraciones Públicas competentes se vigilará la calidad permanente de los productos en el mercado, así como la adecuación de los procedimientos de fabricación, control y almacenamiento seguidos por las Empresas.
1. La distribución y venta al público de los condones podrá efectuarse a través de las oficinas de farmacia y demás establecimientos abiertos al público quedando prohibida su venta ambulante.
También podrá efectuarse su venta mediante máquinas automáticas expendedoras concebidas al efecto. En todo caso, los establecimientos, locales y máquinas expendedoras en los que se efectúe su venta, deberán reunir las condiciones que garanticen la integridad y mantenimiento de las características técnicas y sanitarias del artículo.
2. El suministro, distribución y venta estarán sometidos a inspección y vigilancia sanitaria. A tal efecto sus responsables comunicarán previamente su existencia y actividad a las Autoridades Sanitarias de las Comunidades Autónomas. Esta declaración de actividad no será de aplicación a las Oficinas de Farmacia.
La publicidad de los condones se ajustará a lo establecido en la Orden de 10 de diciembre de 1985 por la que se regulan los mensajes publicitarios referidos a medicamentos y determinados productos sanitarios.
Tendrán la consideración de infracciones sanitarias a lo dispuesto en el presente Reglamento las acciones y omisiones previstas en el artículo 35 de la Ley 14/1986, de 25 de abril, General de Sanidad, y específicamente las siguientes:
1. Infracciones leves:
1.ª La distribución y venta de preservativos de caucho sin efectuar la comunicación a que se refiere el artículo 10.2.
2. Infracciones graves:
1.ª La fabricación o comercialización de preservativos que no se ajusten a las condiciones determinadas en el proceso de su homologación.
2.ª La realización de ofertas, promociones o publicidad que contravengan lo dispuesto en las normas generales y específicas que regulan estos aspectos.
3.ª La falta de comunicación de las situaciones a que se refiere el artículo 4.º
4.ª La expendición de preservativos en condiciones que no garanticen la integridad y el mantenimiento de sus características técnicas y sanitarias.
5.ª El incumplimiento de los requisitos relativos al embalaje y etiquetado de los preservativos.
3. Infracciones muy graves:
1.ª La comercialización de preservativos de caucho que no se hallen debidamente homologados, o a los que se les haya revocado la homologación.
Las acciones y omisiones constitutivas de infracciones según lo previsto en el artículo 12 de este Reglamento serán objeto de las sanciones administrativas correspondientes, previa instrucción del oportuno expediente, sin perjuicio de las responsabilidades civiles, penales o de otro orden que puedan concurrir.
1. Las infracciones a que se refiere el artículo 12 de este Reglamento serán sancionadas con multa de acuerdo con la graduación establecida en el artículo 36 de la Ley 14/1986, de 25 de abril, General de Sanidad.
2. En todo caso, cuando sean detectadas infracciones de índole sanitaria, el Órgano instructor dará cuenta inmediata de las mismas a las Autoridades Sanitarias, las cuales adoptarán las medidas preventivas que estimen pertinentes según lo previsto en la citada Ley General de Sanidad.
Cuando por hechos contrastados o por nuevos conocimientos científicos, la utilización de alguno de estos productos presente peligro para la salud de las personas, la Dirección General de Farmacia y Productos Sanitarios podrá exigir que dichos productos incluyan en su etiquetado aquellos datos o advertencias que resulten adecuados.
El presente Real Decreto tendrá la condición de norma básica al amparo de lo previsto en el artículo 149.1, decimosexta, de la Constitución Española, y, en los artículos 40.5 y 95, en concordancia con el 2.º, 1, de la Ley 14/1986, de 25 de abril, General de Sanidad, con excepción de los artículos 9.º y 10.2.
Con el fin de que por aplicación del punto 1 del artículo 3.º del presente Real Decreto no se produzcan desabastecimientos en el mercado, mientras la Dirección General de Farmacia y Productos Sanitarios procede a la homologación de los condones de caucho, se fija un plazo de un año como límite para la distribución y comercialización de artículos sin homologar, a partir de la entrada en vigor del presente Real Decreto.
1. A partir de la entrada en vigor del presente Real Decreto quedan derogadas las disposiciones que se citan:
– Real Decreto 3033/1978, de 15 de diciembre, en lo que se oponga a lo dispuesto en el presente.
– La Orden de 8 de julio de 1988 («Boletín Oficial del Estado» del 21), por la que se declara Norma Oficial la Norma UNE 53-625-89.
2. Asimismo, se derogan cuantas disposiciones de igual o inferior rango se opongan a lo establecido en el presente Real Decreto.
A los efectos previstos en el artículo 2.º, 2, la Dirección General de Farmacia y Productos Sanitarios procederá, mediante Resolución, a la modificación del anexo I del presente Real Decreto.
Se autoriza a la Dirección General de Farmacia y Productos Sanitarios para establecer los textos relativos a las instrucciones de conservación, uso y desecho, así como los referentes a la prevención de enfermedades de transmisión sexual que deben acompañar al preservativo.
El presente Real Decreto entrará en vigor al día siguiente de su publicación en el «Boletín Oficial del Estado».
Dado en Madrid a 22 de noviembre de 1991.
JUAN CARLOS R.
El Ministro de Seguridad y Consumo,
JULIÁN GARCÍA VALVERDE
CARACTERÍSTICAS Y MÉTODOS DE ENSAYO
(UNE 53-625-89)
1. Objeto y campo de aplicación.
Esta norma especifica los requisitos exigibles a los preservativos de caucho de un solo uso, como las características y los métodos de ensayo. Además indica las condiciones de etiquetado de los mismos.
Queda excluido del campo de aplicación de esta norma toda referencia a la eficacia de los espermicidas y otras sustancias complementarias.
2. Normas para consulta.
UNE 66-020.—Inspección y recepción por atributos. Procedimientos y tablas.
3. Definiciones.
3.1 Preservativo (condón): Un preservativo (condón) es una funda delgada, flexible, diseñada para ser usada sobre el pene en erección durante las relaciones sexuales, con el fin de impedir que el esperma penetre en la vagina y ayudar a prevenir enfermedades de transmisión sexual. También puede utilizarse para la recogida de semen.
3.2 Lote de fabricación: Es un número de preservativos producidos durante un período determinado de tiempo, en un ciclo de fabricación, proceso o serie de procesos bajo condiciones esencialmente iguales. La característica fundamental de un lote de fabricación es su homogeneidad.
3.3 Clave de identificación del lote: Es la contraseña idéntica en todos los ejemplares que identifica el lote de fabricación.
3.4 Lote de inspección: Conjunto de unidades, como máximo 150.000, de producto del que se extrae una muestra para inspección, con objeto de determinar su conformidad con criterios de aceptabilidad.
4. Materiales y clasificación según su diseño.
4.1 Materiales y diseño:
Los preservativos deberán estar fabricados a partir de un compuesto de caucho vulcanizado que les permita satisfacer las especificaciones de la presente norma y estar exentos de impurezas en su masa.
Los preservativos y cualquier material complementario aplicado a éstos no deberán contener ni liberar sustancias que sean reconocidas como tóxicas, susceptibles de producir alergias o irritaciones o que puedan ser nocivas bajo condiciones de uso normales. El lubricante, polvo o cualquier otro material añadido, no deberá causar deterioro al preservativo.
El extremo abierto del preservativo debe terminar en un burlete que bordee toda la circunferencia.
NOTA.–Los preservativos pueden ser transparentes, traslúcidos, opacos o coloreados.
4.2 Clasificación según su diseño:
Los preservativos incluidos en esta norma se clasifican en las clases y tipos siguientes:
Clase 1: 52 milímetros de anchura nominal.
Clase 2: 49 milímetros de anchura nominal.
Tipo A: Superficie lisa.
Tipo B: Superficie rugosa (texturada).
NOTA.–Los preservativos pueden ser secos o lubricados, con o sin depósito.
5. Especificaciones.
5.1 Especificaciones dimensionales:
5.1.1 Muestreo. La toma de muestras de cada lote de inspección se realizará según la norma UNE 66-020 nivel de inspección especial S-2.
5.1.2 Las especificaciones dimensionales estarán de acuerdo con lo indicado en la tabla 1.
TABLA 1
Especificaciones dimensionales
|
Preservativos |
Longitud mínima (mm) (véase 6.1) |
Anchura (mm) hasta 85 mm desde el extremo abierto (véase 6.2) |
Masa máxima (g) (véase 6.3) |
NCA* |
|
|---|---|---|---|---|---|
|
Clase |
Tipo |
||||
|
1 |
A |
160 |
52 ± 2 |
1.7 |
4.0 |
|
|
B |
160 |
52 ± 2 |
2.0 |
4.0 |
|
2 |
A |
150 |
49 ± 2 |
1.5 |
4.0 |
|
|
B |
150 |
49 ± 2 |
1.8 |
4.0 |
|
(*) NCA: Nivel de calidad aceptable (véase la norma UNE 66-020). |
|||||
El NCA se aplica a todos los preservativos que no satisfacen alguna de las exigencias dimensionales.
5.2 Características físicas:
5.2.1 Resistencia. Se puede determinar por uno o por los dos métodos siguientes, según convengan las partes interesadas.
5.2.1.1 Resistencia a la tracción:
5.2.1.1.1 Muestreo. La toma de muestras de cada lote de inspección se realizará según la norma UNE 66-020 nivel de inspección especial S-2.
5.2.1.1.2 La resistencia a la tracción mínima deberá ser 17 MPa (1) y el alargamiento mínimo en la rotura del 650 por 100, utilizando un NCA de 2,5 que se aplicará a todos los preservativos que no satisfagan alguna de las propiedades en tracción.
5.2.1.2 Volumen y presión de explosión:
(1) 1 MPa = 1 N/milímetro cuadrado.
5.2.1.2.1 Muestreo. La toma de muestras de cada lote de inspección se realizará según la norma UNE 66-020 nivel de inspección especial S-2.
5.2.1.2.2 El volumen y la presión de explosión de los preservativos suministrados estarán de acuerdo con lo indicado en la tabla 2.
5.2.2 Ausencia de agujeros y zonas porosas:
5.2.2.1 Muestreo. Las muestras se tomarán de cada lote de inspección, de acuerdo con la norma UNE 66-020 nivel de inspección general 1.
TABLA 2
Volumen y presión de explosión
|
Volumen de explosión mínimo (dm3) (véase 6.5) |
Presión de explosión mínima (kPa) (véase 6.5) |
NCA* |
|
|---|---|---|---|
|
Clase 1 |
Clase 2 |
||
|
15 |
13 |
0,9 |
2,5 |
(*) El NCA se aplica a todos los preservativos que no satisfacen alguna de las exigencias de volumen o presión de explosión.
5.2.2.2 Cuando los preservativos se ensayan según el apartado 6.6, se aplicará un NCA de 0,4.
Si los preservativos se suministran a granel, se someterán al ensayo de detección de agujeros y zonas porosas después de ser colocados en los envases unitarios.
5.2.3 Estabilidad del color de los preservativos pigmentados:
5.2.3.1 Muestreo. Las muestras se tomarán de cada lote de inspección, de acuerdo con la norma UNE 66-020 nivel de inspección S-2, aplicando un NCA de 1,0.
5.2.3.2 Cuando los preservativos se ensayan según el apartado 6.7, no deberán presentar señales de tinción sobre papel absorbente.
Nota.–Es esencial que este ensayo se realice sobre preservativos colocados en envases unitarios. tal como se suministran para la venta.
5.3 Estabilidad durante el almacenamiento:
Cuando los preservativos se someten al ensayo de envejecimiento acelerado, tal y como se describe en el capítulo 7, el volumen de explosión deberá ser, como mínimo, de 12 decímetros cúbicos para la clase 1, y de 11 decímetros cúbicos para los de la clase 2, y la presión de explosión debe ser de 0,8 kPa para ambas clases, utilizando en todos los casos un NCA 2,5.
La resistencia a la tracción mínima deberá ser 15 MPa y el alargamiento mínimo en el momento de la rotura del 600 por 100, utilizando en ambos casos un NCA de 2,5 y un nivel de inspección S-2.
NOTA.–Los elastómeros tienden a deteriorarse con el tiempo. Los preservativos se envasarán de tal manera que queden protegidos durante el almacenamiento; se almacenarán en lugar seco y fresco y permanecerán envasados para no sufrir ningún deterioro mecánico o por acción de la luz. Todos los preservativos que presenten algún deterioro (por ejemplo viscosidad y fragilidad) en el elastómero, deberán ser destruidos e incluidos en los resultados de ensayo.
Los preservativos no deberán estar en contacto con antisépticos a base de aceites, fenoles o sus derivados, grasas derivadas del petróleo, gasolina, querosenos y derivados.
6. Métodos de ensayo.
6.1 Determinación de la longitud:
6.1.1 Fundamento del ensayo. Se suspende libremente el preservativo desenrollado sobre un mandril graduado y se lee la longitud, excluyendo el depósito.
6.1.2 Aparatos necesarios:
6.1.2.1 Mandril. Un mandril provisto de una regla graduada en milímetros y que tenga las medidas indicadas en la figura 1.
6.1.3 Procedimiento operatorio:
6.1.3.1 Se desenrolla el preservativo y se estira ligeramente dos veces para alisar las posibles arrugas causadas por el enrollado.
6.1.3.2 Se coloca el preservativo sobre el mandril y se supende libremente, estirado solamente por su propio peso.
6.1.3.3 Se anota el valor más pequeño redondeando al milímetro más próximo que pueda ser leído sobre la regla graduada que sobresale del extremo del preservativo.
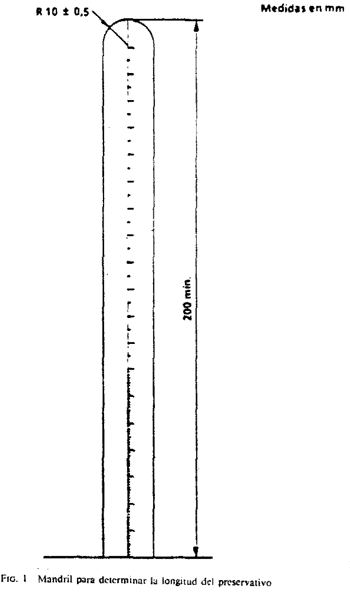
6.1.4 Informe: En el informe se hará constar:
a) Identificación de la muestra.
b) Longitud medida según el apartado 6.1.3.3.
c) Fecha del ensayo.
6.2 Determinación de la anchura:
6.2.1 Fundamento del ensayo. Se suspende libremente el preservativo desenrollado sobre el borde de una regla y se lee su anchura.
6.2.2 Aparatos necesarios:
6.2.2.1 Regla de acero graduada en milímetros.
6.2.3 Procedimiento operatorio:
6.2.3.1 Se desenrolla el preservativo y se pone plano sobre el borde de la regla, dejándolo colgar libremente.
6.2.3.2 Se mide la anchura en un punto cualquiera, situado a una distancia de, como máximo, 85 milímetros del extremo abierto y se anota esta anchura redondeando al milímetro más próximo. En los preservativos que tengan una parte con una anchura superior cercana al extremo cerrado, también se medirá ésta y se anotará.
6.2.4 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Anchura medida según el apartado 6.2.3.2.
c) Fecha del ensayo.
6.3 Determinación de la masa:
6.3.1 Fundamento del ensayo. Se determina la masa de un preservativo utilizando una balanza.
6.3.2 Aparatos necesarios:
6.3.2.1 Balanza. Una balanza con una precisión de 0,01 gramos.
6.3.3 Procedimiento operatorio:
6.3.3.1 Se pesa el preservativo en la balanza y se anota la masa redondeando al 0,1 gramos más próximo.
6.3.3.2 En el caso de preservativos fabricados o empolvados que excedan el límite especificado en la tabla 1, se determinará la masa neta después de haber extraído el lubricante o polvo, lavando el preservativo con una cantidad mínima de propanol-2 y secándolo durante dieciséis horas, como mínimo, a temperatura ambiente; después se pesa según el apartado 6.3.3.1.
6.3.4 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Masa determinada según los apartados 6.3.3.1 ó 6.3.3.2, anotando el método utilizado.
c) Fecha del ensayo.
6.4 Determinación de las propiedades de resistencia a la tracción:
Este ensayo sólo es aplicable a los preservativos que tengan una superficie lisa suficientemente grande situada a más de 90 milímetros del extremo abierto que permite obtener una probeta de 20 milímetros de anchura.
6.4.1 Fundamento del ensayo. Se corta una probeta del preservativo y se estira hasta el punto de rotura, y a continuación se mide la resistencia a la tracción y el alargamiento en la rotura.
6.4.2 Aparatos necesarios:
6.4.2.1 Dispositivo de corte, formado por dos cuchillas paralelas separadas por una distancia de 20 ± 0,1 milímetros, montadas en una troqueladora sobre una placa convenientemente plastificada. La longitud de la parte cortante de cada cuchilla no deberá ser inferior a 70 milímetros.
6.4.2.2 Micrómetro con esfera graduada, colocado en posición vertical en un soporte rígido sobre una base plana. La esfera deberá estar graduada preferentemente en 0,001 milímetros. El micrómetro deberá presentar una superficie de contacto de un diámetro comprendido entre 3 y 7 milímetros, perpendicular al piston y paralelo a la base.
6.4.2.3 Máquina de tracción, sin inercia, que permita ejercer una fuerza transversal a velocidad constante y satisfacer las exigencias siguientes:
a) Las tensiones de la probeta deben ser equilibradas, ya sea por rotación mecánica de un rodillo o bien por lubrificación de las superficies cilíndricas de los rodillos con un material que no afecta al elastómero. Si se gira mecánicamente el rodillo, su frecuencia de rotación deberá ser aproximadamente 7 min-1.
b) Una capacidad de carga de 0 a 100 N.
c) Una velocidad de separación de rodillos de 8,5 ± 0,8 milímetros/segundo (500 ± 50 milímetros/min).
d) Un registro manual o automático de la distancia de separación de los rodillos y de la fuerza durante el ensayo.
6.4.3 Preparación de las probetas. Se coloca el preservativo plano, con su longitud en ángulo recto respecto a las cuchillas del dispositivo de corte y se obtiene la probeta cortando de una sola vez en una zona situada a 80 milímetros del extremo abierto. Solamente se utilizarán las probetas que hayan sido separadas al dar el primer corte. Se lava la probeta cuidadosamente con una cantidad suficiente de propanol-2 para retirar cualquier sustancia añadida y se deja secar, como mínimo, durante dieciséis horas.
6.4.4 Procedimiento operatorio. Se mide el espesor de pared de la probeta en cuatro puntos equidistantes con una aproximación de, como mínimo, 0,001 milímetros alrededor del borde. Se espolvorea la probeta con polvos de talco, se coloca plana y se mide la distancia entre los bordes doblados con una aproximación de 0,1 milímetros. A continuación se coloca la probeta sobre los rodillos y se estira hasta que se rompa. En el momento de rotura se mide la carga aplicada con una aproximación de 0,1 N y la distancia de separación (entre los ejes de los rodillos), con una aproximación de 1 milímetro.
A medida que la muestra se vaya estirando en la máquina de tracción, si se ve un corte defectuoso u otra irregularidad (corte, raja, etcétera) antes del 300 por 100 de alargamiento, la probeta debe ser desechada y no incluida en los resultados de los ensayos.
6.4.5 Expresión de resultados. La resistencia a la tracción, T, expresada en megapascales, de cada probeta, viene dada por la fórmula siguiente:
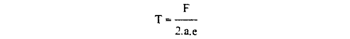
donde
F es la carga de rotura, expresada en newtons;
a es la anchura de la probeta, expresada en milímetros (20 milímetros);
El resultado se redondeará al 0,5 MPa más próximo.
El alargamiento en la rotura E se expresará para cada probeta en tanto por ciento y viene dado por la fórmula:

donde
El resultado debe ser redondeado al 10 por 100 más próximo.
6.4.6 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Número de muestras ensayadas.
c) Resistencia a la tracción y alargamiento en la rotura de cada probeta.
d) Fecha del ensayo.
6.5 Determinación del volumen y de la presión de explosión:
6.5.1 Fundamento del ensayo. Se hincha con aire una longitud constante del preservativo y se anota el volumen y la presión en el momento de la explosión.
6.5.2 Aparatos necesarios:
6.5.2.1 Sistema de alimentación (véase figura 2). Que permita hinchar el preservativo con aire limpio con un caudal medio durante el ensayo de 24 a 30 dm3/min. Este caudal se podrá calcular a partir del volumen de explosión y de la duración del ensayo. La influencia de la variación de la presión sobre el cálculo del caudal será desechada. Un sistema apropiado bloqueará la alimentación de aire cuando la explosión se produzca.
6.5.2.2 Medidor de presión apropiado que permita medir la presión con una aproximación de ± 0,02 kPa. La medida de la presión se podrá realizar en un lugar conveniente de la tubería de alimentación que permita desechar la pérdida de carga entre el punto de medida y el preservativo.
6.5.2.3 Medidor de volumen apropiado que permita medir el volumen con una aproximación de ± 0,2 dm3. La influencia de la variación de presión sobre la medida del volumen será desechada.
6.5.2.4 Varilla de 140 milímetros de longitud que tenga en un extremo una superficie esférica lisa de 20 milímetros de diámetro (véase figura 2) para suspender el preservativo desenrollado cuando se fija en el aparato.
6.5.3 Procedimiento operatorio:
6.5.3.1 Se desenrolla el preservativo y se suspende sobre la varilla fijándolo al aparato y se hincha con aire a una velocidad de 0,4 a 0,5 dm3/s (24 a 30 dm3/min).
6.5.3.2 Se mide y registra el volumen de explosión en decímetros cúbicos redondeando al 0,5 dm3 más próximo, y la presión de explosión en kilopascales redondeando al 0,1 kPa más próximo.
6.5.4 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Volumen y presión de explosión para cada preservativo ensayado.
c) Fecha del ensayo.
6.6 Detección de agujeros y zonas porosas:
La detección de agujeros y zonas porosas se realizará por uno de los métodos siguientes:
6.6.1 Método A:
6.6.1.1 Fundamento del ensayo. Se llena el preservativo con un volumen de agua determinado y se examina a fin detectar cualquier escape de agua visible a través de la pared del preservativo suspendido.
6.6.1.2 Aparatos necesarios:
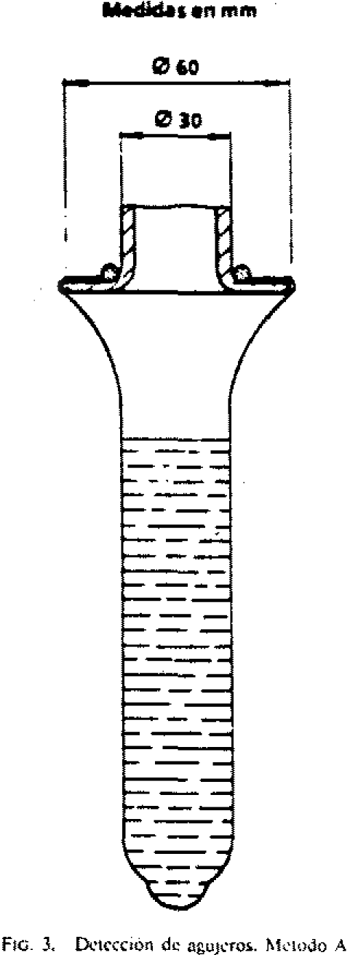
6.6.1.2.1 Equipo adecuado para suspender el preservativo por un extremo abierto (véase figura 3).
6.6.1.2.2 Medios para llenar el preservativo con agua a temperatura ambiente.
6.6.1.2.3 Plataforma para apoyar el preservativo lleno cuando sea necesario.
6.6.1.3 Procedimiento operatorio. Se desenrolla el preservativo y se fija sobre su extremo abierto en el equipo (véase apartado 6.6.1.2.1) quedando suspendido con el extremo abierto hacia arriba. Se llena con 300 cm3 de agua a temperatura ambiente o si no fuera posible, con el volumen máximo que acepte y se examina, como mínimo, durante tres minutos para ver si hay escapa de agua en una distancia de 125 milímetros desde el extremo cerrado.
Si debido a la distensión del preservativo el agua no llega a los 125 milímetros del extremo cerrado, se elevará éste con la ayuda de la plataforma hasta que el nivel de agua alcance esta distancia. Después de tres minutos se examina nuevamente la parte que contiene agua para observar cualquier escape.

En el caso de preservativos lubricados debe eliminarse previamente el lubricante con propanol-2.
6.6.1.4 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Existencia de escape de agua en las condiciones fijadas.
c) Fecha del ensayo.
6.6.2 Método B:
6.6.2.1 Fundamento del ensayo. El ensayo se basa esencialmente en un método de conductividad.
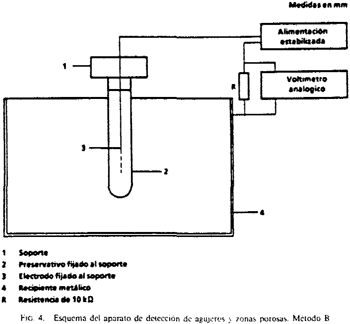
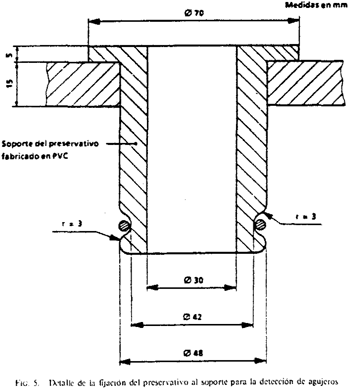
6.6.2.2 Aparatos necesarios. Para la realización de este ensayo se utilizará un aparato cuyo esquema se indica en la figura 4.
El soporte será de poli (cloruro de vinilo). En la figura 5 se indica de una manera detallada la fijación del preservativo al soporte.
Se utilizará también una solución salina compuesta por agua en la que se ha disuelto 1 por 100 en masa de cloruro sódico.
6.6.2.3 Procedimiento operatorio. Se llena el recipiente metálico con la solución salina y se coloca en serie, entre éste y el electrodo, una fuente de corriente continua estabilizada en 10 V, con una resistencia eléctrica de 10 kΩ. A continuación se fija el preservativo al soporte, se llena de solución salina y se introduce rápidamente en el recipiente hasta que queden sumergidas las tres/cuartas partes en la solución salina y se realizan las medidas en los diez segundos siguientes.
6.6.2.4 Expresión de los resultados:
6.6.2.4.1 Si el preservativo no presenta ninguna fuga, no pasa corriente en el circuito eléctrico y se comporta como si fuera aislante entre el electrodo y el recipiente metálico. Si por el contrario el preservativo presenta una fuga, hay paso de corriente eléctrica a través de la solución salina entre el recipiente y el electrodo.
6.6.2.4.2 Se considera que un preservativo presenta fuga si sometido a una tensión de 10 V se produce una tensión igual o superior a 0,050 V medida en los bordes de la resistencia de 10 kΩ.
6.6.2.5 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Indicación de las fugas eventuales reveladas por el método de la medida de la conductividad después del ensayo con agua.
c) Fecha del ensayo.
6.6.3 Destrucción de los preservativos. Los preservativos sometidos a este ensayo serán destruidos.
6.7 Determinación de la estabilidad del color:
6.7.1 Fundamento del método. Se moja el preservativo completamente con agua destilada y se envuelve en papel blanco absorbente. Después de un período de tiempo se examina el papel para observar señales de tinción.
6.7.2 Aparatos necesarios:
6.7.2.1 Papel absorbente blanco.
6.7.2.2 Recipiente adecuado para evitar pérdida de humedad durante el tiempo que dura el ensayo.
6.7.3 Procedimiento operatorio. Se moja por dentro y por fuera el preservativo con agua destilada, sin extraer las sustancias añadidas, si las hubiera. Se envuelve el preservativo mojado en papel blanco absorbente de manera que la mayor superficie posible del preservativo esté en contacto con el papel y se pone en el recipiente para evitar la pérdida de humedad. Se deja reposar en el recipiente a temperatura ambiente durante dieciséis a veinticuatro horas.
Después de retirar el papel absorbente se examina éste a simple vista para observar posibles señales de tinción.
6.7.4 Informe. En el informe se hará constar:
a) Identificación de la muestra.
b) Indicación de cualquier señal de tinción en el papel absorbente.
c) Fecha del ensayo.
6.7.5 Destrucción de los preservativos. Los preservativos sometidos a este ensayo deben ser destruidos.
7. Estabilidad durante el almacenamiento.
7.1 Fundamento del método:
Se miden las propiedades en tracción y/o la presión y el volumen de explosión de los preservativos después de acondicionados en sus embalajes a temperatura elevada y durante un tiempo determinado.
7.2 Aparatos necesarios:
7.2.1 Estufa. Una estufa capaz de alcanzar una temperatura de 70 ± 2° C.
7.2.2 Aparatos especificados en los apartados 6.4.2 y 6.5.2.
7.3 Preparación de las muestras:
7.3.1 Los preservativos deben acondicionarse en una estufa durante 48 ± 1 h a 70 ± 2° C en sus envases individuales originales.
7.3.2 Los preservativos suministrados a granel deben ser envasados individualmente, eventualmente con un lubricante apropiado, como si fueran a ser ofrecidos al consumidor, antes de ser sometidos a esta prueba. Los envases deben de ser como se especifica en el capítulo 8.
7.4 Procedimiento operatorio:
Después de acondicionados los preservativos, como se indica en el apartado 7.3.1, se mantienen a 23 ± 2° C durante, como mínimo, doce horas, pero no más de noventa y seis horas. A continuación se abren los envases y se examinan los preservativos para detectar cualquier signo de deterioro como viscosidad, fragilidad u otros.
En ese mismo plazo se miden las propiedades en tracción, según se especifica en el apartado 6.4, y/o del volumen y presión de explosión, según se especifica en el apartado 6.5.
7.5 Expresión de resultados:
Se calcula y registra la resistencia a la tracción y el alargamiento en el punto de rotura, como se describe en el apartado 6.4, y/o se anota el volumen y presión de explosión, como se describre en el apartado 6.5.
7.6 Informe:
En el informe se hará constar:
a) Identificación de la muestra.
b) Número de muestras ensayadas.
c) Descripción de cualquier deterioro visible en los preservativos después de su acondicionamiento.
d) Valores de resistencia a la tracción y alargamiento en el punto de rotura y/o volumen y presión de explosión.
e) Fecha del ensayo.
8. Embalaje y etiquetado.
8.1 Muestreo:
La toma de muestras de cada lote de inspección se realizará según la norma UNE 66-020, nivel de inspección especial S-2, utilizando un NCA de 2,5.
8.2 Embalaje:
Cada preservativo deberá ser colocado en un envase cerrado, estanco, en condiciones higiénicas satisfactorias. Varios envases individuales pueden empaquetarse juntos en un mismo envase múltiple.
Si se utiliza tinta para marcar el preservativo o cualquier parte del envase en contacto con él, no debe, en ningún caso, causar deterioro al preservativo o ser nocivo para el consumidor.
El diseño de los envases individuales o múltiples y los materiales de que están compuestos, serán tales que protejan perfectamente los preservativos durante el transporte y almacenamiento, y no sufran daño mecánico al abrir el paquete o envase.
Cuando los envases múltiples no sean preparados por el fabricante, es deseable que el responsable del empaquetado conserve los datos necesarios para poder averiguar el origen del producto.
El material del envase no debe enmohecerse en climas tropicales ni atraer a los insectos.
8.3 Etiquetado:
8.3.1 En el envase individual deben figurar los datos siguientes:
a) Identificación del fabricante, importador o acondicionador (nombre o marca comercial y otra referencia que lo identifique).
b) Número de lote de fabricación.
8.3.2 En el envase múltiple figurarán los siguientes datos:
a) Identificación del producto: Marca comercial.
b) Nombre del fabricante y del importador o acondicionador, según proceda.
c) Número de preservativos que contiene.
d) Descripción del artículo: Clase, tipo, con o sin depósito, lubricado o no, y color. La clase y tipo pueden indicarse mediante las letras o número correspondiente o mediante la característica o medida a que hagan referencia.
e) Número de lote de fabricación.
f) Fecha de caducidad (mes y año), no debe ser superior a cinco años.
g) Instrucciones de uso y conservación, pueden figurar en hoja aparte incluida en el envase.
h) Referencia a la norma UNE 53-625.
Don ................................................................................................................................,
con domicilio en ......................................................, provincia de .......................................,
calle ................................................................................................, número .......................
con DNI número ......................................................., como propietario o en representación
de (1) ...................................................................................................................................,
legalmente establecido en ..................................................., código postal .........................,
provincia de ............................................................., calle ..................................................,
.........................................................................................................., número .....................,
teléfono/fax ...........................................................................................................................
EXPONE: Que desea homologar el preservativo de caucho:
Marca comercial Número unidades/caja
Fabricado por (2) ...........................................................................................................
Controlada su calidad (2) ...............................................................................................
Envasado por (2) ............................................................................................................
Importado por (2) ............................................................................................................
CARACTERÍSTICAS DEL PRESERVATIVO
Clase ............................................................., tipo ..............................................................,
con o sin depósito ................................................................................................................
Sustancias añadidas:
Espermicida .................................................. composición .............................................
........................................................................
Lubricante ..................................................... composición .............................................
........................................................................
Otros (función) ............................................... composición ..............................................
........................................................................
Colores que puede presentar ........................................................................................
Fecha de caducidad ......................................................................................................
A estos efectos acompaña a este escrito la documentación preceptiva.
............................ a ........... de ........................ de ........
EL SOLICITANTE,
Fdo.:
(1) Firma fabricante o importadora.
(2) Incluir nombre y dirección.
Agencia Estatal Boletín Oficial del Estado
Avda. de Manoteras, 54 - 28050 Madrid